Esta vieja conocida mía, por el tiempo que lleva formando parte de una de mis listas, parece haber comenzado el despertar de su largo letargo que a punto estuvo de llevarla al mismísimo averno en su momento; Consiguió la aprobación de Gelclair por parte la FDA, un medicamento que puede ayudar a cientos de miles de personas que padecen cáncer con inflamaciones dolorosas y ulceraciones en la superficie de la boca y garganta, lo que pudiera ser una definición para andar por casa de la mucositis oral, mal para el que puede servir de paliativo contra el dolor, esta droga comercializada en forma de gel.
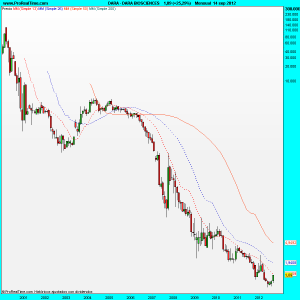
Os voy a poner el gráfico en velas mensuales en logarítmico, solo para que se pueda observar que una de las acciones actuales (no son las antiguas, ¡ojo!), llegó a valer ¡mas de 125.000 dólares!; ¡De traca!.
La explicación la encontramos como es lógico en un split 1:16 el 13 de mayo de 2010 pasando de tener en circulación casi 200 millones de títulos a los actuales 11.930.000 lo que viene a ser una importante diferencia.
Pero en fin, con ello se salvo de la quema y desde entonces parece haber enfocado debidamente el asunto de la financiación y lo que es mas importante, pudiera haber encontrado el camino correcto, que lo lleve a una aprobación en su momento por parte de la todopoderosa FDA, de sus drogas en fase desarrollo, amén de la que ya tiene (Gelclair) aprobada para el tratamiento de la mucositis oral y que DARA planea lanzar en el primer trimestre de 2013 y para lo que ha llegado a un acuerdo con el grupo suizo Helsinn Grants, para la distribución en USA, acuerdo que le irá suponiendo según ventas, unas importantes y suculentas «regalías» monetarias.
………………….
Una vez que os supongo situados mas o menos, sobre lo que estamos hablando y su teórico potencial, paso directamente a enseñaros como andan sus gráficas tanto en semanal como en diario y lo que pueden traernos a partir de aquí.
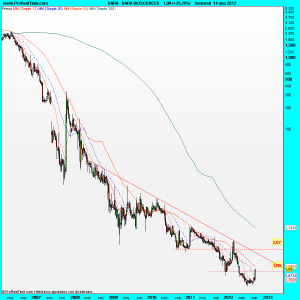
En semanal tengo que seguir trabajando con el mismo en logarítmico, porque de otra forma sería muy complicado tener una imagen nítida y sobre todo proporcional sobre el momento donde se encuentra el precio.
No perdáis el norte sobre su realidad y sobre sus posibilidades como le de por subir, ya que igual no nos da tiempo ni a verlo; En serio, tener en cuenta para situaros, que si dividimos entre 16 la cotización (recordad split 1:16), nos encontraríamos con un cierre el viernes a pesar de la subida en ¡atención! de 0,068 dólares por acción, habiendo llegado a unos mínimos según este parámetro de 0,038 $ por cromo; ¡De cine ¿verdad?!.
Bueno los niveles por lo demás están claros en el gráfico, ha superado una importante resistencia, dejando atrás ese dólar por papeleta tan importante en nasdaq, la siguiente la tenemos por encima de dos dólares y por medio hay otro escollo, esa bajista que viene desde mayo de 2008.
…………………
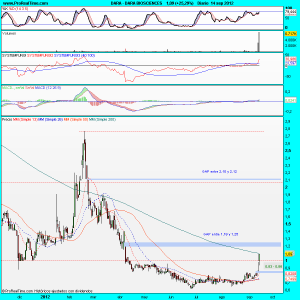
En diario, en esta ocasión ya en lineal, vemos otras muchas cosas: Tenemos «gaps» por arriba y por debajo, unos nos servirán como resistencias a batir y otro como soporte a no perforar; No quiero dejar pasar la ocasión sin comentar un pensamiento que siempre me hago cuando un precio sube así de rápido, como es el hecho de observar como un precio que apenas mueve 100.000 títulos de media diaria, pasa a mover millones en las últimas dos jornadas; Me pregunto, ¿la noticia que ha supuesto este movimiento es para tanto?, ¿puede durar en el tiempo?.
Eso es lo que tendrán que evaluar aquellos que contemplen este precio como potencial miembro de su cartera, ya que eso no puedo hacerlo yo; Hasta aquí llego, a partir de aquí, continua vuestro dedo.
Eso si, este es uno de esos precios que como le de por subir, no deben sorprendernos porcentualidades centenarias.
…………………………
ACTUALIZADO 30 DE SEPTIEMBRE DE 2012.
……………….
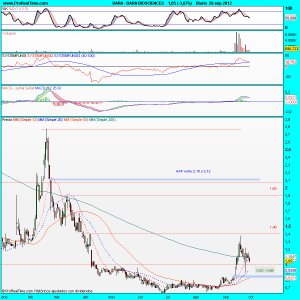
Os actualizo el gráfico a cierre del viernes.
………………….
Superfungi,muchísimas gracias por el seguimiento del valor.A ver que nos depara esta semana.Yo estoy seguro que jugosas plusvalías,,
Un saludo y suerte Diego.
Pues amigo Diego, parece que va a empezar a empujar; De momento está cubriendo el primer «gap»; Si lo consigue el siguiente objetivo será 1,40$
Suerte, que pinta muy bien.
Hola. Teneis pensado entrar? Es que he leido por ahi que tiene buenas espectativas.
un articulo traducido de hoy:
El pasado noviembre de 2012, DARA Biosciences ( DARA ) anunció que ha presentado una solicitud a la FDA de los EE.UU. solicitando la designación de fármaco huérfano en KRN5500 para el tratamiento de la neuropatía periférica inducida por quimioterapia crónica ( CCIPN ) . Ha pasado más de un año desde que la sumisión , y que puede asustar a algunos inversores a creer que toda esperanza está perdida. Después de todo , el propio objetivo de la FDA para responder a las solicitudes de medicamentos huérfanos es de 75 días, y lo que va de 2013 el 91% han sido menos de 90 días. Pero sabemos a ciencia cierta que DARA y la FDA han estado yendo atrás y adelante en la aplicación. Creemos que esto es debido al tamaño global del mercado CCIPN .
Discutimos esto más adelante , y la conclusión de que la falta de noticias sobre el estado de la aplicación no nos concierne . De hecho , ahora que hemos eclipsado trece meses desde que la presentación original, pensamos que una decisión puede ser inminente , y por DARA Bio , pensamos que esto podría ser un gran catalizador positivo e importante para la re- valoración de las acciones a un significativamente mayor nivel.
Medicamentos Huérfanos – ¿Qué son / lo que no son
La FDA de los EE.UU. estableció la Ley de Medicamentos Huérfanos (AOD ) en enero de 1983 . La AOD ya se ha mejorado y ampliado , con el objetivo de animar a las empresas farmacéuticas y de biotecnología para desarrollar medicamentos para enfermedades raras. Según la ley, las compañías que desarrollan un medicamento para un trastorno que afecta a menos de 200.000 personas en los Estados Unidos pueden vender sin competencia durante siete años, así como obtener algunos incentivos fiscales del ensayo clínico. Designación huérfana también califica el desarrollador de drogas para una exención de la cuota de utilización de medicamentos recetados. Más sobre la Ley de Medicamentos Huérfanos de la FDA se puede encontrar en el sitio web de la FDA.
En la práctica , las ventajas fiscales y exención de cuotas de los usuarios son de mucha mayor importancia a las pequeñas empresas de biotecnología , pre – ingresos que a las grandes empresas farmacéuticas. Para este último grupo , las principales consideraciones son la garantía de exclusividad en el mercado y la etiqueta de medicamento huérfano , que puede ser vista como proveedora de la validación de la FDA de que la población del medicamento tiene como objetivo tratar es sustancialmente lo suficientemente pequeño para que las empresas pueden cobrar materialmente más por la droga que una indicación para el mercado masivo .
La designación de fármaco huérfano no es , sin embargo , una aprobación por parte de la FDA de que el fármaco será un éxito de taquilla , o incluso llegar al mercado . Medicamentos huérfanos pueden fallar en los ensayos clínicos al igual que no los medicamentos huérfanos . Dicho esto , hemos escrito recientemente un informe que muestra que los medicamentos huérfanos tienen más probabilidades de tener éxito en los ensayos clínicos en fase inicial en comparación con los fármacos sin la designación de medicamento huérfano . Obras demuestra que los medicamentos huérfanos tenían éxito ensayos de fase 3 y lo hizo a través de la aprobación final de la FDA el 58% de las veces, en comparación con 49 % para los medicamentos no huérfanos. Eso es una estadística interesante , porque a pesar de la designación de fármaco huérfano no es un endoso por el organismo en la eficacia, los medicamentos huérfanos son alrededor de un quinto más probabilidades de éxito que los medicamentos no huérfanos. Los medicamentos huérfanos no oncológicos se aprueban 68 % de las veces .
Pronto una decisión sobre KRN5500 ?
DARA Bio ha desarrollado KRN5500 durante casi una década. Es una de las últimas piezas que quedan de la vieja DARA Bio desde antes de la nueva administración asumió el cargo en diciembre de 2011 y dramáticamente cambió el enfoque de la compañía de las oportunidades del mercado de masas en la diabetes , el cáncer y las enfermedades autoinmunes en el foco actual de la atención de apoyo oncológico. KRN5500 un derivado semisintético intravenosa del espicamicina antibiótico antineoplásico nucleósido como , originalmente aislado de la bacteria Streptomyces alanosinicus . Tiene el potencial para ser un gran avance , la medicina no opioides para el tratamiento del dolor neuropático en pacientes con cáncer , o más específicamente , la neuropatía inducida por quimioterapia crónica periférica ( CCIPN ) .
KRN5500 fue desarrollado originalmente por la japonesa Kirin Brewery , en un esfuerzo para identificar nuevos agentes anti – cáncer que inducen la apoptosis y la diferenciación de células de leucemia mieloide . El trabajo fue realizado en colaboración con el Hospital General de Massachusetts (MGH ), el Instituto Nacional del Cáncer (NCI ) y el Eastern Cooperative Oncology Group (OTC: ECOG ) en los datos de EE.UU. preclínicos demostraron que KRN5500 tiene significativa actividad in vitro contra linfocítica crónica humana leucemia de células (LLC ), proporcionando así un apoyo para el avance en los estudios clínicos para los pacientes con LLC , así como aquellos con leucemia mieloide aguda (LMA ) y los tumores sólidos.
Cuatro ensayos clínicos se han realizado en pacientes con cáncer , incluyendo uno en Japón y tres en los EE.UU. Un total de 91 pacientes con tumores sólidos han sido tratados con dosis únicas IV KRN5500 de hasta 21 mg/m2 y dosis semanales de hasta 42 mg / m2. Desafortunadamente , no se observó ninguna respuesta antitumoral objetivo a la dosis máxima tolerada (DMT ) en cualquiera de estos programas . Sin embargo , se observó la reducción del dolor neuropático potente en un número significativo de pacientes . MGH publicó estos datos en Clinical Cancer Research en noviembre de 2003 . Un análisis adicional de estos hallazgos fue publicado en el Journal of Pain y tratamiento de los síntomas , en abril de 2012.
Basándose en estos hallazgos , KRN5500 fue reformulado , específicamente para eliminar excipientes que causaron efectos secundarios gastrointestinales en los ensayos de cáncer de originales , y el desarrollo se ha avanzado en CCIPN . CCIPN es un tipo de dolor que resulta de daño en los nervios y se caracteriza por una hipersensibilidad anormal a inocua , así como los estímulos nocivos . Este tipo de dolor es extremadamente difícil de manejar , no responde a las intervenciones analgésicos estándar, incluyendo los opioides , y con frecuencia empeora con el tiempo . Actualmente no hay tratamientos aprobados por la FDA para CCIPN . Dado el vacío en el mercado y los datos revisados por expertos que apoyan la utilidad potencial de la droga, la FDA de EE.UU. concedió la condición de vía rápida para KRN5500 en CCIPN .
Vemos CCIPN como una buena oportunidad de mercado para DARA Bio . El mercado global del dolor neuropático es enorme, prevé que crezca a $ 6 mil millones en 2015 . Es uno de los mercados más codiciados en la industria farmacéutica , y fármaco huérfano hace la oportunidad aún más atractivo dado los siete años de exclusividad de mercado indicadas anteriormente . Específico para esta oportunidad , el dolor neuropático se produce en el 30% de los pacientes de cáncer , incluyendo hasta 90 % de los pacientes con cáncer avanzado . La incidencia y la gravedad de CCIPN varían considerablemente para cada agente neurotóxico , administrado solo o en combinación , pero para vincristina , cisplatino , oxaliplatino , y paclitaxel , las estimaciones son tan altas como 70 % a 90 % . Tanto como el 60 % de los pacientes que recibieron docetaxel y 40 % de los tratados con carboplatino desarrollan CCIPN .
Según la Sociedad Americana del Cáncer, se estima que hay 12 millones de estadounidenses que viven con cáncer activo y cerca de 1,6 millones de casos nuevos cada año . No todos los tipos de cáncer resulta en dolor neuropático , y no todos los pacientes con cáncer son activos en la quimioterapia . Pero de forma conservadora , si suponemos que la mitad de 30 % se indicó anteriormente con dolor neuropático son debido a la quimioterapia y otros agentes neurotóxicos , la oportunidad de mercado para KRN5500 es de alrededor de 1,8 millones de pacientes !
Es evidente que esto es mayor que el máximo permitido de 200.000 bajo la Ley de Medicamentos Huérfanos . Por lo tanto , la aplicación de DARA recorta algunos refractario u otro subconjunto de esta población a caer por debajo del máximo de 200.000 . Desde la presentación original de nuevo en noviembre de 2012 , DARA ha estado en comunicación activa con la FDA. Creemos que ha habido varios intercambios de correspondencia » ida y vuelta » entre DARA y el FDA que hacen a mano el texto exacto de la indicación. De hecho, si nos fijamos en el comunicado de prensa de DARA para el tercer trimestre de 2013, señaló que la gestión de la empresa respondió a una solicitud de información de la agencia el 10 de septiembre de 2013 y la información adicional se presentará en noviembre de 2013 . Sólo podemos asumir que esta información adicional se ha presentado , y la FDA a responder de nuevo a DARA en 75 días. Así que, aunque la aplicación DARA Bio KRN5500 es cada vez un poco largo en el diente , siempre y cuando el diálogo continúa , somos optimistas sobre el resultado .
Los datos apoyan Moving Forward
El 8 de septiembre de 2010, DARA Bio presentó los resultados positivos del estudio a partir de un estudio de escalada de dosis 2a fase con KRN5500 en el 13 º Congreso Mundial sobre el Dolor . El estudio multicéntrico, fase 2a controlado con placebo, fue diseñado para evaluar la seguridad y eficacia de KRN5500 para el tratamiento del dolor neuropático en pacientes con cáncer. El ensayo comparó KRN550 frente a placebo para determinar las diferencias de tratamiento en mediana de los cambios desde el inicio en las puntuaciones de dolor registrados por los pacientes en un diario todos los días según se mide por la escala de puntuación numérica ( NRS ) . Los resultados muestran :
KRN5500 redujo significativamente el dolor neuropático , en comparación con placebo ( 24 % vs 0 %, p = 0,03 ) cuando se mira en la mediana de disminución en la intensidad del dolor desde la línea base .
KRN5500 significativa mejora en el número de pacientes que consiguieron una reducción del dolor desde la línea de base de > 20 % en comparación con el placebo ( 83 % vs 29 %, p = 0,04 ) .
KRN5500 redujo significativamente NRS desde la línea base en comparación con el placebo cuando se mira en la mejor respuesta media a la semana ( 29,5 % vs 0 %, p = 0,02 ) .
Además , el análisis de regresión de la mejor respuesta para cada paciente a lo largo dosis mostró una disminución significativa en la intensidad del dolor lineal con aumento de la dosis ( pendiente = -18,2 , p = 0,009 ) .
Estos resultados indican que KRN5500 fue eficaz en la reducción del dolor en pacientes con CCIPN de una manera dependiente de la dosis . Las dosis más altas de KRN5500 resultan en una mayor reducción en el dolor a través del tiempo . Los datos fueron publicados en el Journal of Pain y tratamiento de los síntomas , en abril de 2012 ( documento completo ) .
En mayo de 2012 , DARA ha anunciado nuevos datos del estudio de fase 2a que incorporó un nuevo análisis realizado por un experto en bioestadística externo con amplia experiencia FDA. Previo análisis de los datos del estudio se basan predominantemente en Numeric Rating Scale ( NRS ) las puntuaciones de dolor informadas por los pacientes recogidos por profesionales de la salud en una clínica en las visitas semanales , mientras que este nuevo análisis se centró específicamente en las puntuaciones de dolor diario de auto-reporte de los diarios de los pacientes . Los respondedores en este análisis se definieron como pacientes alcanzar una mejoría clínicamente significativa – (al menos 20 %) en las puntuaciones de NRS medio desde el inicio dentro de cualquier semana dada.
De los 12 pacientes que recibieron KRN5500 en este estudio 19 pacientes, 7 ( 58 % ) fueron clasificados como respondedores . Además, 5 de la 7 ( 71 % ) mostraron un alivio del dolor sostenida durante varias semanas . De los 7 pacientes que recibieron placebo, ninguno fue respondedores. Consideramos que estos resultados impresionantes ya que los pacientes inscritos en este estudio de prueba de concepto tenía dolor implacable al inicio del estudio a pesar del uso concomitante de otros agentes analgésicos aprobados.
KRN5500 fue generalmente bien tolerado con reacciones adversas a (GI) los síntomas principalmente gastrointestinales , tales como náuseas , vómitos y diarrea limitados. Y éstos eran más frecuentes y graves en el brazo KRN5500 que en el grupo placebo. Trastornos GI afectados 11 ( 92 % ) de los 12 pacientes dosificados con KRN5500 frente a sólo 4 ( 57 % ) para el placebo . De hecho , un tercio de los trastornos GI relacionadas con KRN5500 se considerará que ser graves . Sin embargo , la gestión de DARA ha atribuido estos síntomas a los excipientes tales como DMAC y monoetanolamina utilizado en la formulación original de KRN5500 conocido para inducir náuseas y vómitos . Hojas de Datos de Seguridad del Material sobre estos dos compuestos en cuenta esta ocurrencia ( 1 , 2 ) . En consecuencia, DARA ha reformulado desde KRN5500 para eliminar estos excipientes y reducir estos efectos secundarios gastrointestinales relacionados . DARA hace mención de esto brevemente en su más reciente Formulario 10Q .
Con huérfano Designación Viene un socio
En abril de 2010 , DARA Bio anunció que ha firmado un acuerdo de ensayos clínicos sobre KRN5500 con la División de Prevención del Cáncer ( DCP ), el Instituto Nacional del Cáncer , de los Institutos Nacionales de Salud ( NIH), para el tratamiento de CCIPN en pacientes con cáncer. Bajo los términos de la colaboración , el NCI ayudará a financiar las futuras etapas de desarrollo . También sospechamos que DARA puede aprovechar la red del NCI estableció nacional de investigadores (Programa Comunitario de Oncología Clínica – CCOP ) para llevar a cabo los estudios futuros.
Pero la colaboración a solas con el NCI , incluso con apoyo financiero, no es suficiente para financiar un programa de fase 2b en CCIPN . Incluso con la ayuda del Instituto Nacional del Cáncer , estamos buscando en $ 6 a $ 8 millones para hacer este trabajo . DARA no tiene que mucho disponible para gastar . Por lo tanto , esperamos que DARA asociarse KRN5500 a los pocos meses de la decisión de la FDA para conceder la condición de huérfano . La dirección nos ha dicho que están en conversaciones con socios potenciales en KRN5500 , y que una sociedad no es necesariamente supeditada a la decisión de fármaco huérfano de la FDA. Si bien creemos que esto es alentador, DARA Bio ha estado teniendo estas discusiones de los últimos tres años. En nuestra opinión, obtener el estatus de medicamento huérfano para KRN5500 es el factor decisivo para si o no KRN5500 es una droga partnerable .
La razón principal por la que creemos designación de fármaco huérfano es el portero de una asociación es la inminente expiración de la protección de patentes en torno a la droga. En los documentos presentados por DARA Bio , la empresa señala seis patentes activas que protegen KRN5500 . Encontramos US- 5 , 461,036 , presentada en julio de 1992 por el Kirin Beer Kabushiki Kasha , «derivados espicamicina y su uso como agentes contra el cáncer «, como la patente más antigua . También presentamos por Kirin en 1995 fue US- 5 , 631,238 , en el uso de derivados espicamicina . Ambos de estas patentes han expirado ya . En mayo de 1999 , MGH fue concedido un método de utilización de la patente US- 5 , 905,069 en adelante, «Reducir o prevenir el dolor usando espicamicina o derivados de los mismos . » Sobre la base de la fecha de prioridad , asumimos esta patente expira en 2018 , a menos que DARA Bio puede obtener la aprobación antes del vencimiento , en cuyo caso se les concedería una prórroga adicional de cinco años bajo la legislación Hatch -Waxman .
Otras patentes propiedad de la MGH son US- 7 , 196071 , y las aplicaciones relacionadas US- 7 , 375,094 y US- 7 , 632,825 . La patente ‘071 se presentó en septiembre de 2001 como » métodos para disminuir o prevenir el dolor usando derivados espicamicina . » Creemos que estos pacientes protegerán KRN5500 hasta el 2021 o el 2022. DARA Bio ha presentado dos nuevas aplicaciones que demandan nuevas formulaciones de derivados espicamicina y protegen los métodos para el alivio del dolor . Estas dos patentes tienen por objeto proteger KRN55500 hasta el año 2029 y 2032 , sino como una patente de formulación , pueden no proporcionar una alta barrera a la entrada de genéricos .
Si se dificulta la evaluación de la exclusividad de mercado exacto de KRN5500 dado que la composición de las patentes de la materia han expirado. Método de uso de patentes se mantienen activos por lo menos hasta 2018, con la ventaja de 2022. Sin embargo , DARA Bio tiene que obtener la aprobación de KRN5500 antes de la expiración de las patentes ‘069 o genéricos empresas pueden ser capaces de desafiar a los tres siguientes en ‘071 , ‘094 y ‘825 patentes con evidencia. Dado el estado de ‘ Fast Track ‘, que puede ser posible, pero la falta de plazos de exclusividad de mercado claras puede ser lo que se ha mantenido hasta la firma de una alianza de la droga hasta la fecha. Las compañías farmacéuticas pueden ser atraídos por el tamaño del mercado y los datos sobre KRN5500 generados por DARA Bio en el estudio fase 2a , pero no van a gastar millones de empujar la droga sólo hacia adelante para luchar contra la competencia de genéricos posteriormente unos años después de su lanzamiento .
Las dos patentes de formulación presentados por DARA que tienen como objetivo proteger el uso hasta el año 2029 o 2032 son atractivos en longitud, pero aún no se han hecho y es casi seguro que ser desafiado posterior a la aprobación . Por último , la legislación Hatch -Waxman proporcionará cinco años de exclusividad si KRN5500 llega al mercado. Eso es casi en el límite para la mayoría de las compañías farmacéuticas para gastar o no gastar en una droga. Es por esto que creemos fármaco huérfano es tan importante para DARA . Socios farmacéuticos obtendrían un extra de dos años garantizados, sin batallas legales y los desafíos de párrafo IV ANDA . Elimina lo que vemos como la mayor proyección de firmar un acuerdo por el medicamento.
conclusión
Más recientemente Escribimos sobre DARA Bio que la historia de la oncología de la especialidad que nos atrajo a las acciones de hace un año se mantiene intacta , pero la paciencia fue requerido por los inversionistas porque las cosas se están moviendo más lento de lo esperado. La principal razón de la lenta implantación de los productos clave de la compañía era una sustancial fuerza de talla inferior a las ventas. En 2013, DARA ha tenido problemas para vender lo que los médicos y los pacientes no saben que existe. Parte de la mente de DARA Bio sigue siendo baja. Por lo tanto , estamos encantados de ver a la empresa la adopción de las medidas adecuadas para ampliar la fuerza de ventas y step-up promoción tanto Soltamox y Gelclair en 2014.
KRN5500 ha sido sobre todo una idea de último momento en nuestra tesis de inversión que se centra en los activos comerciales centrales de la compañía en Soltamox , Gelclair y Bionect . Sin embargo , el estatus de medicamento huérfano para KRN5500 cambia las cosas – que crea una enorme boca procedente de la tubería, así como las asociaciones . Una sociedad es algo que podría venir con un pago por adelantado y el desarrollo hito importante que DARA puede utilizar para continuar con la expansión y la intensificación de la promoción de los bienes comerciales. Ya tenemos dara ritmo Bio a ‘ Comprar’ con un objetivo de $ 1.50. Conseguir la designación de fármaco huérfano para KRN5500 convierte este potencial triples en un home run. Es una historia de cambio embellecer en el 2014 , si todo se junta .
Ahora DARA no se encuentra claramente en una pérdida sin estatus de fármaco huérfano en KRN5500 . Queremos que esto quede claro . KRN5500 siempre ha sido al revés de la historia comercial de la oncología especialidad ya existentes. Creemos que los cambios DARA Bio hizo a la promoción a principios de año han permitido claramente a la empresa a ganar tracción . Las ventas en el tercer trimestre de 2013 aumentaron 80 % en forma secuencial a partir del segundo trimestre de 2013. A principios de este mes , DARA Bio anunció que la inscripción en el registro de la captura de la compañía se ha completado, y DARA espera utilizar los datos de este registro para impulsar las ventas de Soltamox en 2014. Creemos que hay un camino a la rentabilidad en el horizonte. Al precio de hoy , los inversores son cada vez KRN5500 gratis .
Pero si la FDA otorga la designación de medicamento huérfano para KRN5500 y la empresa puede obtener un socio para la fase 2b , pensamos acciones DARA Bio están posicionados para un movimiento significativo superior. El valor actual de mercado es de sólo $ 15 millones. KRN5500 un potencial fármaco $ 250 millones en CCIPN . El pago por adelantado solo de un potencial interesado podría duplicar las acciones. Las investigaciones demuestran que los medicamentos huérfanos tienden a tener éxito en mayor proporción que no Medicamentos Huérfanos , y la FDA ha declarado un objetivo de responder a todas las solicitudes en 75 días. DARA ha presentado una respuesta a las preguntas de la agencia el 10 de septiembre de 2013. Los datos adicionales fueron proporcionados a la agencia en noviembre de 2013 . Esperamos una decisión en el próximo mes o dos, y creemos que podría ser un importante catalizador para la re- valoración de un nivel superior .
http://seekingalpha.com/article/1900351-orphan-designation-a-game-changer-for-dara?source=yahoo
os dejo enlace
Al parecer han realizado un reverse split. La valoracion que tenia ha bajado. Que supone para los que tenemos acciones de Dara?
Alguno puede explicar el tema del reverse split de DARA?
Gracias.
superfungi para cuando una actualización? gracias
DARA BioSciences’ KRN5500 Receives Orphan Drug Designation From FDA
Read more: http://www.nasdaq.com/press-release/dara-biosciences-krn5500-receives-orphan-drug-designation-from-fda-20140225-00434#ixzz2uLiH4rrU
DARA super algo gordo se está cociendo. Actualiza cuando puedas. Mira el volumen en mensual
DARA
Hoy resultados al cierre y mañana, antes de apertura, conferencia de prensa.
Empresa con una caja de unos 14 kilos a 30/09/2014, con una quema trimestral de unos 2 kilos, sin deuda y con varios
productos a la venta (ultimo trimestre 600.000 dolares de venta, en este 4° trimestre de 2014 se esperan 750.000 dolares, lo que supondría unos 3 millones anuales) y una fase 2b con designación de medicamento huérfano.
Cuanto diriais q vale? Pues no, menos, solo 18 millones (19,5 millones de acciones).
La veo como una interesante oportunidad.
Del lado técnico el súper la ve muy mal, pero TODO ES POSIBLE, no?
Estoy dentro a 0,97.